In diesem Artikel wird aus Gründen der besseren Lesbarkeit das generische Maskulinum verwendet. Weibliche und anderweitige Geschlechteridentitäten werden dabei ausdrücklich mitgemeint, soweit es für die Aussage erforderlich ist.
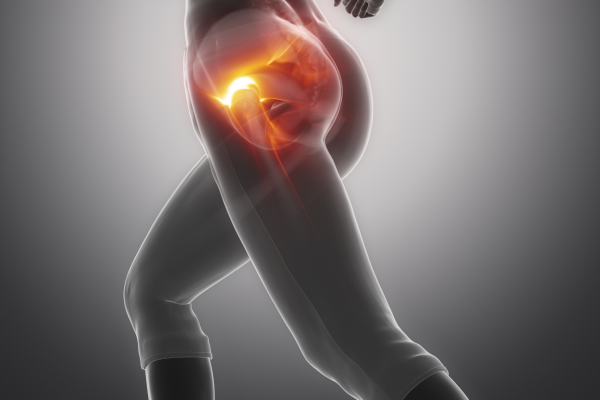
Hüftschmerzen und Sehnenbeschwerden sind ein häufiges Problem sowohl bei Sportlern als auch bei Nicht-Sportlern. Schmerzen in der Hüfte können viele Ursachen haben. Befindet sich dein Schmerz eher auf der Innenseite, schau gerne bei unseren Blogbeiträgen (Adduktorenvereltzung, Schambeinentzündung) vorbei. In diesem Beitrag geht es um den seitlichen (äußeren) Hüftschmerz, in der Literatur auch gluteale Tendinopathie, greater trochanteric bursitis oder greater trochanteric pain Syndrom genannt (mehr dazu unter Punkt 1). Bis zu jede vierte Frau im mittleren Lebensalter ist davon betroffen. Das Vorkommen der Gesamtbevölkerung liegt bei 10% bis 25% (Del Buono et al., 2011). Die Schmerzen sind meist belastungsabhängig und können negative Auswirkungen auf die sportliche Leistung, Lebensfähigkeit und Arbeitsfähigkeit haben (Albers et al., 2016). Was du dagegen tun kannst, erfährst du jetzt.
1. Terminologie – Was steckt hinter den Namen?
Für seitlich lokalisierte Hüftschmerzen mit einer punktuellen Empfindlichkeit über dem Trochanter major (Rollhügel des Hüftgelenks) findet man in der Literatur verschiedene Terminologien (Namen). Es wird beispielsweise als Bursitis Trochanterica diagnostiziert, dies kann unangemessen sein, da nur drei der vier Entzündungszeichen Rötung, Schwellung, Wärme und Schmerz vorhanden sind. Der Schmerz steht häufig im Vordergrund, auch ohne andere Zeichen der Entzündung (Reid, 2016).

Bildgebende Befunde bei Patienten mit Trochanterschmerzsyndrom (GTPS) weisen eine unterschiedliche Häufigkeit an klinischen Veränderungen auf. Eine Schleimbeutelentzündungen (Bursitis trochanterica) kommt bei 4 % und 46 % vor und eine Tendinopathien der Gesäßmuskulatur (Gluteale Tendinopathie) zwischen 18 % und 50 % (Reid, 2016). Diese spezifischen Bezeichnungen weisen also gegebenenfalls auf eine Erkrankung hin, die nicht vorliegt. Daher ist der bevorzugte klinische Begriff für Schmerzen im äußeren Hüftbereich in aktuellerer Literatur Trochanterschmerzsyndrom (greater trochantic pain syndrom „GTPS“) (Reid, 2016). Dieser wird in diesem Beitrag verwendet.
2. Was ist es?
Das GTPS beschreibt Schmerzen im seitlichen äußeren Hüftbereich, die u.a. verstärkt werden können durch einbeinige Belastungen wie Einbeinstandaktivitäten, Joggen und durch manuellen Druck oder durch Druck in der Seitlage (Reid, 2016).
Veränderungen der Sehne (Tendinopathien) können die Ursache für die Schmerzen sein. Es kann zu erhöhter Zellbildung und Proteinbildung, Einsprossung von neuen Gefäßen und Veränderungen der Zellbestandteile (Desorganisation der Matrix) kommen. Allerdings liegt nicht immer eine Entzündung zugrunde. Teilweise findet man in der Literatur Hinweise auf eine mögliche entzündliche Komponente. Man geht davon aus, dass der Entstehungsmechnaismus der Veränderungen beim GTPS multifaktoriell ist und der genaue Mechanismus nicht bekannt ist. Ähnlich wie bei anderen Sehnenbeschwerden kann ein Hauptfaktor eine Überlastung durch eine zu geringe Ausgangssituation oder eine Überlastung durch eine Phase mit plötzlicher, deutlich gesteigerter Aktivität der Sehne sein (Adduktorenverletzungen, Achillessehnenriss).

Anatomischer Hintergrund:
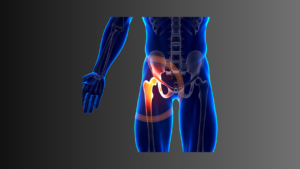
Der Trochanter major ist ein großer viereckiger Vorsprung an der Verbindung zwischen Oberschenkelhals und Schaft. Er ist der Hauptansatzpunkt für die starken Abduktorensehnen, der Muskeln die das Bein in die Abduktion (nach außen) bewegen. Schleimbeutel in dem Bereich, dienen dazu Reibungen zu verringern, um Bewegungen in engen Bereichen zu puffern. Es kann etwa 20 Schleimbeutel im Trochanterbereich geben, denn es können einige Schleimbeutel aufgrund von übermäßiger Reibung erworben werden. Drei Schleimbeutel (Bursae) sind bei der Mehrheit der Menschen im Trochanterbereich vorhanden. Dazu gehört die Bursa gluteus minimus, Bursa subgluteus medius und die Bursa subgluteus maximus, welcher der größte Schleimbeutel und oft als „Trochanterschleimbeutel“ bezeichnet wird. Er liegt seitlich des Trochanter major zwischen dem Gluteus medius und dem maximus (Gesäßmuskulatur). Teile der Gesäßmuskulatur sind maßgeblich daran beteiligt das Hüftgelenk zu stabilisieren, v.a. auch im Einbeinstand. Risse der Glutealsehne treten bei etwa 22 % der älteren Patienten auf (Reid, 2016).
3. Wer ist davon betroffen?
Die Prävalenz von einseitigem und beidseitigem GTPS betrug 15,0 % und 8,5 % bei Frauen und 6,6 % und 1,9 % bei Männern. Die höhere Prävalenz des GTPS bei Frauen deutet darauf hin, dass eine veränderte Biomechanik der unteren Extremität mit dem GTPS in Zusammenhang stehen könnte. Man vermutet, dass das breitere Becken der Frau damit zu tun haben könnte. Andere Faktoren müssen mit der Entwicklung des GTPS in Zusammenhang stehen, da nicht jede Frau ein GTPS entwickelt. Es ist daher naheliegend, dass das GTPS von vielen verschiedenen Faktoren abhängt. Das Geschlecht selbst scheint allerdings ein Risikofaktor zu sein. Betroffen sind vor allem Frauen im Alter zwischen 40 und 60 Jahren (Segal et al., 2007, Reid, 2016, Almekinders et al., 2003, Del Buono et al., 2011).
4. Wie wird es diagnostiziert?
In der ärztlichen oder physiotherapeutischen Untersuchung können schmerzhafte Sehnen ertastet werden im Bereich des Trochanter Major, außerdem kann der Einbeinstand seitliche Hüftschmerzen provozieren. In einer Untersuchung mit geringer Stichprobe (n=65) wurden diese beiden Tests näher untersucht. Bei Probanden mit nachgewiesenen GTPS im MRT führte man beide Tests durch. Nachweislich ist es unwahrscheinlich, dass Patienten mit seitlichen Hüftschmerzen, die über dem Trochanter major nicht tastbar sind, ein GTPS im MRT nachgewiesen haben. Des Weiteren geben die Ergebnisse Hinweise darauf, dass ein Patient, der nach 30 Sekunden Einbeinstand Schmerzen in der lateralen Hüfte hat, mit einer hohen Wahrscheinlichkeit ein GTPS im MRT nachgewiesen hat. Der Einbeinstand und das Tasten der Sehnenansätze scheinen daher einen Aufschluss über das Vorhandensein eines GTPS zu geben. 31% der Probanden waren klinisch negativ, wiesen allerdings ein GTPS im MRT auf (Grimaldi et al., 2017).

Ein MRT kann also sinnvoll sein, um die Ergebnisse der klinischen Untersuchung zu bestätigen. Ultraschall kann ebenfalls genutzt werden, allerdings können hier Sehnenrisse deutlicher dargestellt werden, dagegen sind Veränderungen der Sehnen nicht zuverlässig darstellbar im Bereich des Trochanters (Fearon et al., 2010).
Einige Fragebögen können zur Verlaufskontrolle der funktionellen Einschränkungen durch die Erkrankung genutzt werden. Das VISA-G ist die bevorzugte verfügbare Option zur Erfassung der mit der Gesäßsehnenerkrankung verbundenen Einschränkungen (Nasser et al., 2022, Ebert et al., 2019).
Weitere Tests in der klinischen Untersuchung können durchgeführt werden, um andere mögliche Erkrankungen wie Arthrose, Hüftimpingement oder Adduktorenbeschwerden auszuschließen (Reiman et al., 2015). Hier findest du weitere Informationen zu den Erkrankungen (Adduktorenverletzungen, Schambeinentzündung, Hüftimpingement)
5. Wie bekommst du es in den Griff?
Die Behandlung von Sehnenerkrankungen, also auch des GTPS während der Saison, ist eine Herausforderung für alle Mediziner und Therapeuten. Viele der Strategien, die zur Behandlung von Sehnenerkrankungen in der Rehabilitation eingesetzt werden, sind aufgrund der langen Dauer nicht geeignet. Es sind Managementstrategien erforderlich, die die Schmerzen kontrollieren und die Leistungsfähigkeit erhalten. Dazu gehört ein Belastungsmanagement, das sowohl die Verringerung verschlimmernder Belastungen als auch die Einführung schmerzlindernder Belastungen vorsieht. Dazu können Medikamente eingesetzt werden und eine angemessene Überwachung ist ausschlaggebend, um eine Verschlechterung zu erkennen. Andere Maßnahmen wie Injektionstherapien und andere direkte Sehnenbehandlungen können im schlimmsten Fall provozierend und im besten Fall wirkungslos sein (Cook & Purdam, 2013).
Die Forschung zur Verbesserung des Verständnisses des Managements bei Sportlern in der Saison wird durch ethische Erwägungen und den Zugang zu freiwilligen Teilnehmern beeinträchtigt. Es kann sein, dass hier klinische Erkenntnisse und Fortschritte die zukünftige Behandlung leiten werden. In Nachfolgender Tabelle werden die Behandlungsoptionen der konservativen Behandlung genauer betrachtet. Diese beinhalten schmerzlindernde Medikamente (NSAIDs), Physiotherapie, Stoßwellentherapie und Kortikosteroidinjektionen. Bei den meisten Patienten werden die Symptome durch konservative Behandlungen behoben (Reid, 2016).

Kortisoninjektionen werden in der Praxis in der Behandlung von Sehnenerkrankungen häufig angewendet. Daher findest du hier noch weitere Studien welche die Anwendung von Kortisonbehandlungen bei GTPS mit verschiedenen Kontrollgruppen untersuchten. In einer Untersuchung wurde Kortisoninjetionen und Schulung plus Bewegung verglichen. Nach 8 Wochen erreichten beide Gruppen selbsteingeschätzte Verbesserung der Funktion und Schmerzlinderung im Vergleich zu keiner Behandlung. Nach 52 Wochen führte Schulung plus Bewegung zur größeren allgemeinen Verbesserung als die Anwendung von Kortisoninjektion. Die Ergebnisse sprechen ebenfalls für die eher kurzfristige Wirkung der Kortisoninjektion (Mellor et al., 2018). Grimaldi et al. (2017) bestätigt die Schmerzlinderung durch Kortisoninjektionen innerhalb der ersten vier Wochen und beschreibt ebenfalls die Problematik des Wiederauftretens der Schmerzen und dem sinken der Erfolgsquote mit der Zeit. Zudem scheint es auf lange Sicht nicht wirksamer als Abwarten oder Training zu sein. Akute Komplikationen bei Injektionstherapie sind zwar kaum vorhanden, allerdings bestehen nach wie vor Bedenken hinsichtlich möglicher negativer Auswirkungen auf die Sehne (Grimaldi et al., 2017).

Ähnliche Ergebnisse wurden auch bezogen auf die Plasmainjektionen und Stoßwellentherapie in einem systematischen Review mit dreizehn randomisierten kontrollierten Studien gefunden (n=1034). Im Vergleich zur unbehandelten Kontrollgruppe sinken die Schmerzwerte bei Stoßwellentherapie und Plasmainjektionen signifikant nach 1-3 Monaten. Allerdings schnitt keine der beiden Behandlungen nach 6-12 Monaten besser ab als die Kontrollgruppe ohne Behandlung. Strukturiertes Training hatte die höchste Wahrscheinlichkeit, die beste Behandlung für die Verbesserung der funktionellen Ergebnisse zu sein. Sie war die einzige Behandlung, die mit signifikanter Verbesserung nach 1-3 Monaten im Vergleich zur Gruppe ohne Behandlung (Gazendam et al., 2021).
In einer anderen systematischen Untersuchung wurde bei Patienten mit seitlichem Hüftschmerz und Beteiligung des Schleimbeutels herausgefunden, dass konservative traditionelle Therapie wie Physiotherapie den meisten Patienten hilft. Operationen waren effektiv bei hartnäckigen Fällen (Lustenberger et al., 2011).
Zusammenfassend gibt es geringe aussagekräftige Nachweise zu einer wirksamen Therapie bei GTPS. Progressives, strukturiertes Training zur Belastungssteigerung und Kräftigung der Sehnen scheint eine gute Option ohne Risiken zu sein. Dies erwies sich auch bereits bei Sehnenproblematiken an Hüfte, Knie oder dem Fuß als sinnvoll (Patellofemorales Schmerzsyndrom, Adduktorenverletzungen, Schambeinentzündung, Achillessehnentendinopathie, Achillessehnenriss).
6. Workout
Im folgenden siehst du ein Krafttraining für deine Gesäßmuskulatur. Für eine angemessene und individuelle Rehabilitation sollten die Übungen angepasst an dich, dein Ziel und deine Belastbarkeit abgestimmt werden.
Sumo Squat
Curtsy Lunge
Lying Hip Extension
Glute Bridge
Lying Hip Abduction
Clamshell
7. Fazit
Derzeit gibt es kein evidenzbasiertes Protokoll für die Behandlung des GTPS. Die konservative Behandlung, welche vor allem Physiotherapie und Training beinhaltet, ist der Goldstandard für GTPS mit einer Erfolgsquote von über 90 % (Reid, 2016, Del Buono et al., 2011). Die aktive Therapie erwies sich demnach am effektivsten, besonders auf lange Sicht gesehen. Abhängig von deinen Zielen kann zusätzlich zum Krafttraining ein progressives Lauftraining erarbeitet werden, sodass du auch wieder schmerzfrei joggen oder in deine Spielsportart zurück kannst.
Wir helfen dir gerne bei deiner Gestaltung des Trainingsplans im Rahmen deiner Rehabilitation. Komm gerne auf uns zu, wenn du Fragen hast oder Hilfe benötigst.
Dein Physio-Team aus der Karlsruher Oststadt
Unsere weiteren Blog-Artikel


Was manuelle Lymphdrainage (nicht) kann

Gelenkgeräusche – muss man sich Gedanken machen?
Seitlicher Hüftschmerz Update und Deep-Dive

Faszinierend oder fast nicht belegt – Der Faszien-Hype kritisch betrachtet

Von Eisbädern bis Foam Rolling: Was hilft wirklich gegen Muskelkater?

Kreuzbandrehabilitation – Wie lange brauche ich die Unterarmgehstützen?
Wie schief bin ich eigentlich und ist das schlimm?
Quellenangaben:
Albers, I. S., Zwerver, J., Diercks, R. L., Dekker, J. H. & Van den Akker-Scheek, I. (2016, 13. Januar). Incidence and prevalence of lower extremity tendinopathy in a Dutch general practice population: a cross sectional study. BMC Musculoskeletal Disorders, 17(1). https://doi.org/10.1186/s12891-016-0885-2
Almekinders, L. C., Weinhold, P. S. & Maffulli, N. (2003). Compression etiology in tendinopathy. Clinics in Sports Medicine, 22(4), 703–710. https://doi.org/10.1016/s0278-5919(03)00067-x
Cook, J. L. & Purdam, C. R. (2013). The challenge of managing tendinopathy in competing athletes. British Journal of Sports Medicine, 48(7), 506–509. https://doi.org/10.1136/bjsports-2012-092078
Del Buono, A., Papalia, R., Khanduja, V., Denaro, V. & Maffulli, N. (2011, 4. September). Management of the greater trochanteric pain syndrome: a systematic review. British Medical Bulletin, 102(1), 115–131. https://doi.org/10.1093/bmb/ldr038
Ebert, J. R., Fearon, A. M., Smith, A. & Janes, G. C. (2019). Responsiveness of the Victorian Institute for Sport Assessment for Gluteal Tendinopathy (VISA-G), modified Harris hip and Oxford hip scores in patients undergoing hip abductor tendon repair. Musculoskeletal Science and Practice, 43, 1–5. https://doi.org/10.1016/j.msksp.2019.05.005
Fearon, A. M., Scarvell, J. M., Cook, J. L. & Smith, P. N. (2010, Juli). Does Ultrasound Correlate with Surgical or Histologic Findings in Greater Trochanteric Pain Syndrome? A Pilot Study. Clinical Orthopaedics & Related Research, 468(7), 1838–1844. https://doi.org/10.1007/s11999-009-1174-2
Grimaldi A, Mellor R, Nicolson P, et alUtility of clinical tests to diagnose MRI-confirmed gluteal tendinopathy in patients presenting with lateral hip painBritish Journal of Sports Medicine 2017;51:519-524.
Grimaldi AConservative management of lateral hip pain: the future holds promiseBritish Journal of Sports Medicine 2017;51:72-73.
Gazendam, A., Ekhtiari, S., Axelrod, D., Gouveia, K., Gyemi, L., Ayeni, O. & Bhandari, M. (2021). Comparative Efficacy of Nonoperative Treatments for Greater Trochanteric Pain Syndrome: A Systematic Review and Network Meta-Analysis of Randomized Controlled Trials. Clinical Journal of Sport Medicine, 32(4), 427–432. https://doi.org/10.1097/jsm.0000000000000924
Lustenberger, D. P., Ng, V. Y., Best, T. M. & Ellis, T. J. (2011). Efficacy of Treatment of Trochanteric Bursitis: A Systematic Review. Clinical Journal of Sport Medicine, 21(5), 447–453. https://doi.org/10.1097/jsm.0b013e318221299c
Mellor R, Bennell K, Grimaldi A, et alEducation plus exercise versus corticosteroid injection use versus a wait and see approach on global outcome and pain from gluteal tendinopathy: prospective, single blinded, randomised clinical trialBritish Journal of Sports Medicine 2018;52:1464-1472.
Nasser, A. M., Fearon, A. M., Grimaldi, A., Vicenzino, B., Mellor, R., Spencer, T. & Semciw, A. I. (2022, 8. April). Outcome measures in the management of gluteal tendinopathy: a systematic review of their measurement properties. British Journal of Sports Medicine, 56(15), 877–887. https://doi.org/10.1136/bjsports-2021-104548
Reid, D. (2016, März). The management of greater trochanteric pain syndrome: A systematic literature review. Journal of Orthopaedics, 13(1), 15–28. https://doi.org/10.1016/j.jor.2015.12.006
Reiman, M. P., Mather, R. C. & Cook, C. E. (2015). Physical examination tests for hip dysfunction and injury. British Journal of Sports Medicine, 49(6), 357–361. https://doi.org/10.1136/bjsports-2012-091929
Segal, N. A., Felson, D. T., Torner, J. C., Zhu, Y., Curtis, J. R., Niu, J. & Nevitt, M. C. (2007, August). Greater Trochanteric Pain Syndrome: Epidemiology and Associated Factors. Archives of Physical Medicine and Rehabilitation, 88(8), 988–992. https://doi.org/10.1016/j.apmr.2007.04.014